琼脂糖作为固定化酶载体的思考:特性解析与关键性能考量
近年来,酶作为生物催化剂用于药物制品和有机化合物的合成得到了越来越多的普及,其工业应用数量也在迅速增长。通常情况下,酶催化反应在温和的条件下进行,并且由于其高特异性而能够产生较少的副产物。此外,由于低能耗操作和相对简单的下游加工,它们提供了一种更加环保、节能和更具成本效益的技术。然而,使用天然酶作为生物催化剂存在操作条件下稳定性差、产品回收困难、不可能多次重复使用等缺点,限制了酶在工业规模上的应用。
固定化酶技术能够有效解决上述问题,它不仅可以使天然酶得以回收和重复使用,还可以增强或修饰酶的自然特性,提高其选择性、活性和稳定性,使其更适合作为商业生物催化剂。该技术在工业领域中发挥着至关重要的作用,有助于提高酶催化效率、降低生产成本和增加可持续性等诸多优势。
成功的固定化需要载体特性、固定化方式、工艺设计三个方面共同配合。其中,载体作为固定化技术的核心部分,其粒径、比表面积、孔道结构以及亲疏水性、功能基团、间隔臂的性质等对酶活、稳定性、成本效益、规模化生产可行性等方面起到决定性的作用。一个合格的固定化酶载体需要在活性保留、稳定性、传质效率、操作便利性、成本之间取得平衡。琼脂糖作为满足多重要求的成熟载体,已成为应用最广泛的经典载体基质之一。
本文旨在对琼脂糖固定化酶载体的基础特性进行解析,阐述构效关系,指导科学选型。
一、琼脂糖基质的核心特性:性能优势的底层逻辑
1、化学与结构基础
琼脂糖是海藻提取物琼脂中不带电荷的中性部分,是由β-D-半乳糖和 α-3,6-内醚-L半乳糖交替连接组成的线性多糖聚合物。多糖骨架使其具有高度的亲水性、良好的生物相容性和化学惰性。
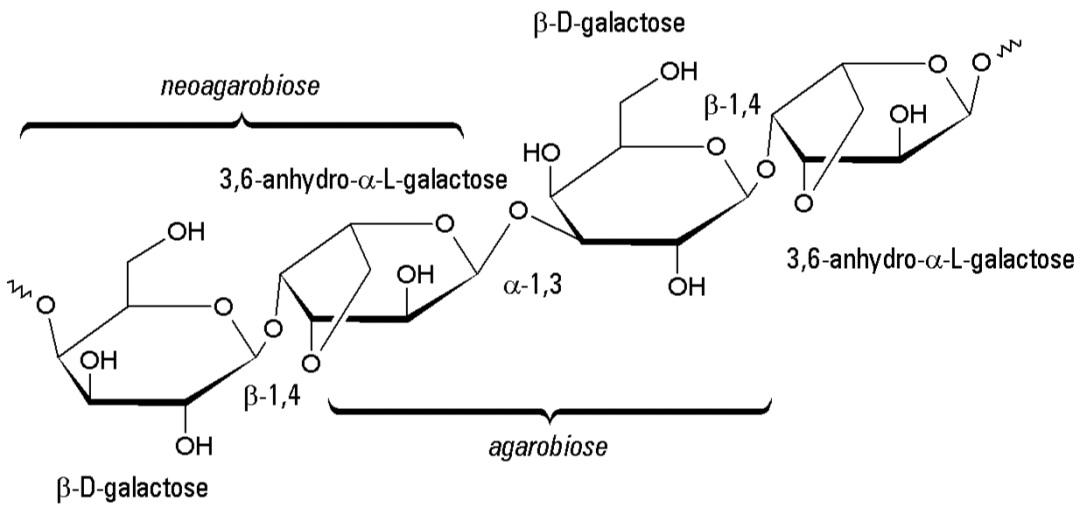
图1 琼脂糖的结构[2]
2、三维网络结构
琼脂糖常温下为白色粉末,不溶于水,加热到80 °C以上才能形成均相的溶液,而冷却至35 °C以下时又可形成稳定的凝胶,这是由于琼脂糖分子与水分子之间的氢键作用所致;目前普遍认为琼脂糖的凝胶机理为:水中的琼脂糖由于羟基的存在,由柔性、无规卷曲的状态逐渐转变为单螺旋、双螺旋的构象变化,双螺旋结构于胶束之间交错形成了3D晶格,而水分子不仅以包裹的形式存在于这些大孔晶格中,还通过氢键进一步稳固凝胶结构。 琼脂糖凝胶不仅具有出色的亲水性,与其他亲水性载体(如聚丙烯酰胺、壳聚糖)相比,该聚合物能够形成可逆的稳定凝胶,且在溶剂变化时不会出现显著的收缩,当凝胶孔中的水分子被丙酮等溶剂替代时,琼脂糖的空间网络结构能够较好地维持。但与聚合物载体相比,琼脂糖裸球的机械强度载体较差,一般需要通过化学交联来提高,常见的交联剂有2,3-二溴丙醇、环氧氯丙烷、二乙烯基砜等[1-3]。
酶固定化过程中,如果想获得高的酶负载量,载体必须具有丰富的比表面积;载体的有效面积(即酶可占据的有效面积)决定了载体结合固定化酶的最大有效负载。但高比表面并不是酶负载的唯一先决条件:只有酶能够进入孔道并与内表面接触,固定化才能进行;因此,除了一定的比表面积,载体还应具有大小合适的开放连通孔道以及高孔隙率,载体孔径足够大时,酶才能够进入孔道内部(孔径大于酶分子的大小)、有足够的空间移动来改变其构象(孔径为酶分子大小的3倍)、并减轻扩散限制(孔径为酶分子大小的8倍);窄分布的载体孔径能够更好地保留酶的活力[1]。载体孔道对底物、产物传质效率的影响同理,并直接影响到催化速率。而交联后的琼脂糖载体不仅具有一定的机械强度,还具有丰富的比表面、高孔隙率、较大且均一的孔道结构,是固定化酶的理想基质。
3、表面化学与可修饰性
琼脂糖表面含有丰富的羟基,为其后续多种活化方式以及对结合位点密度的控制提供了可能。常见的活化方法,如通过环氧氯丙烷对琼脂糖基质同时进行交联强化以及环氧改性;向琼脂糖引入邻位二醇、再经高碘酸盐氧化得到醛基、或直接与戊二醛反应得到带有醛基的琼脂糖载体;还可以进一步与N-羟基琥珀酰亚胺(NHS)、聚乙烯亚胺(PEI)、亚氨基二乙酸(IDA)等进行反应,得到带有氨基、羧基的载体;其中IDA作为配基可与金属离子螯合得到金属螯合亲和介质,这类琼脂糖载体能够选择性捕获并富集那些含有特定氨基酸残基(如组氨酸标签)的蛋白质。氨基化载体还可进一步发生重氮化反应得到重氮盐,定向偶联酶分子。除此之外,十二烷基、丁基和辛基也可以作为疏水配体被添加到琼脂糖载体上,用于脂肪酶的固定化[4]。由此可见,多种活化方式为琼脂糖载体的多种酶固定方式提供了可能。而载体的结合密度则可以通过对具体修饰条件的控制得以实现。
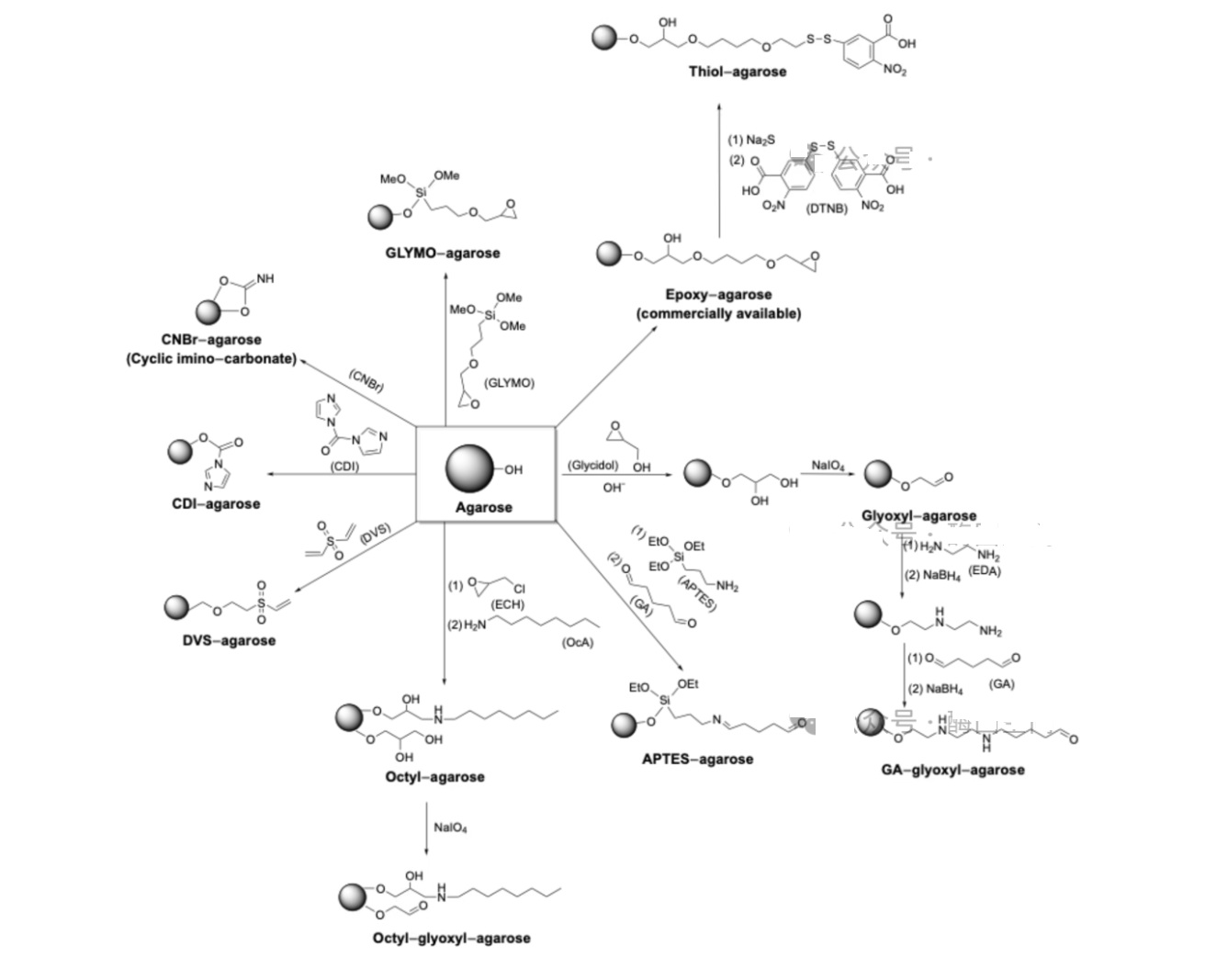
图3 琼脂糖基质的不同化学修饰路线[5]
4、物理化学稳定性
交联强化后的琼脂糖载体具有一定的机械强度,适用于填充式反应器。琼脂糖载体的pH耐受范围较宽,一般长期耐受pH在3-12之间,强酸条件会破坏其3D结构,使用时应尽量注意避免。
二、从特性到性能:构效关系
1、酶高负载潜力与活性保留
琼脂糖固定化酶载体丰富的比表面、合适的孔径、高孔隙率的孔结构特征使其可以为酶分子提供充足的结合位点,这是获得高酶负载量的必要条件。
而琼脂糖载体的亲水环境能够最大程度地模拟酶在水溶液中的状态,减少固定化过程对酶天然构象的破坏,通常可以获得较高的酶活性保留/回收率。也正是因此,琼脂糖载体尤其适用于那些需要温和固定化条件以保持高活性的疏水酶。
此外,功能基团的含量(结合位点密度)也会直接影响到载体表面微环境的性质、酶同载体之间的成键数量,进而影响到固定化酶的负载量、酶活保留及其稳定性选择性。而琼脂糖基质表面丰富的羟基及可化学修饰的特性,使其得以通过对修饰条件的控制实现对载体功能基团含量调控的需求。
2、优秀的操作稳定性
无论是基于经典的非特异性固定化方法(如离子结合、包埋等),还是基于定向固定化方法的琼脂糖固定化酶载体,都能够有效避免酶泄漏的发生,进而保障批次、长期的使用稳定性。此外,良好的机械强度使其能够耐受反应器中的流体剪切力和床层压力,进而延长载体的使用寿命,减轻生产成本。
3、良好的传质效率
合理的孔径大小、高孔隙率、开放连通的骨架结构,有利于减少扩散限制,允许酶、底物/产物分子在载体内部的扩散,进而提高反应效率。
4、可重复使用和成本效益
如上所述,琼脂糖载体具有稳定性高和低浸出的优势,支持其多次重复使用。此外,还有部分载体(如DEAE-琼脂糖、烷基修饰琼脂糖等)可进行再生,从而进一步降低长期使用成本。
琼脂糖固定化酶载体具有诸多优势,而这些优势的实际表现程度高度依赖于载体特性参数的选择,如粒径、孔径、活化基团等,所用载体应与目标酶和实际的使用场景相匹配。
三、科学选型:匹配特性与需求
1、粒径选择
较小粒径的载体具有相对高的比表面积,相应具有较高的酶负载潜力,以及短传质路径带来的高传质效率,但随之带来的还有填充式反应器压降大、易堵塞的问题。因此小粒径载体更适用于分析规模、微反应器或对分辨率要求较高的场景。而大粒径载体(100微米以上)虽然比表面积相对降低,且扩散限制增加进而导致酶活有一定程度的下降,但其压降较低,操作通量高,易分离回收,适用于制备或工业规模的填充床应用。
因此,应综合反应器类型、反应规模、分离方式和压降情况选择合适的载体粒径。
2、孔径选择
首先,为了保证催化能力,选择载体时需确认目标酶分子量、底物/产物分子量,选择具有合适排阻极限的琼脂糖型号。载体孔径应大于酶分子的大小,以确保有效负载,同时也能够匹配底物或产物的尺寸以确保良好的传质效率。此外,载体还应兼具丰富的比表面积和高孔隙率。
3、活化基团的类型及数量
应综合考虑酶表面可利用的功能基团、期望的结合方式、偶联条件及后续的应用环境,以获得理想的固定化酶性能。
带有环氧基团的琼脂糖载体一般不直接用于酶的固定化,这是因为虽然环氧理论上能够与蛋白质多种官能团进行反应,但仅与巯基具有可观的反应活性,且环氧含量一般较低,因此不常直接用于酶的固定化。但可以将一些能够吸附蛋白质的基团(如离子基团,固定化金属螯合物,巯基等)引入到环氧载体上(异功能载体)用于蛋白质固定化。
带有环氧基团的琼脂糖载体经过进一步修饰(如与乙二胺、氨基酸反应),可以在载体表面引入伯胺、羧基官能团,这两类基团均可与酶表面的羧基、氨基完成戊二醛、碳二亚胺介导的偶联[2]。
通过在琼脂糖载体上引入金属螯合配基,可以选择性地捕获并富集那些带有特定功能标签或独特的氨基酸残基的酶,并确保酶在载体上的最佳定向,提高底物的可及性和催化效率。这种方法对于酶活性和选择性至关重要的应用领域尤为重要,例如药物合成或精细化学品生产。有大量文献报道将带有特定氨基酸残基(如组氨酸标签)的蛋白质(如菠萝蛋白酶[6])在温和的条件下定向固定到Cu-IDA-Sepharose等金属螯合琼脂糖载体上,固定化后可显著提高酶的回收率、基质的稳定性、可重复使用性和可再生性。
带有乙醛基的琼脂糖载体可以与酶产生强烈的多点共价附着。其制备路径决定了琼脂糖载体上乙醛基的密度非常高,且乙醛基位阻较低,在碱性条件下具有较高的稳定性(即使在碱性条件下也易于长期储存,甚至可以长期进行酶-支持多重相互作用)[7]。然而,这种固定化方法必须在碱性条件下进行固定,并且需要用硼氢化钠进行最终还原,并将剩余的醛基转化为惰性羟基,但硼氢化物可能对酶(特别是活性中心内含有金属离子的酶)产生一些影响,因此必须严格控制试剂的浓度和用量。
4、供应商考量
载体的质量一致性(批次间粒径、孔径、活化度等关键参数)、产品规格的清晰度(供应商应明确提出产品的粒径、孔径、基团含量等信息)、以及能否提供技术支持(如选型建议,固定化方案参考或问题解答)几个方面都应作为供应商选择的考察范围。
四、典型应用场景举例
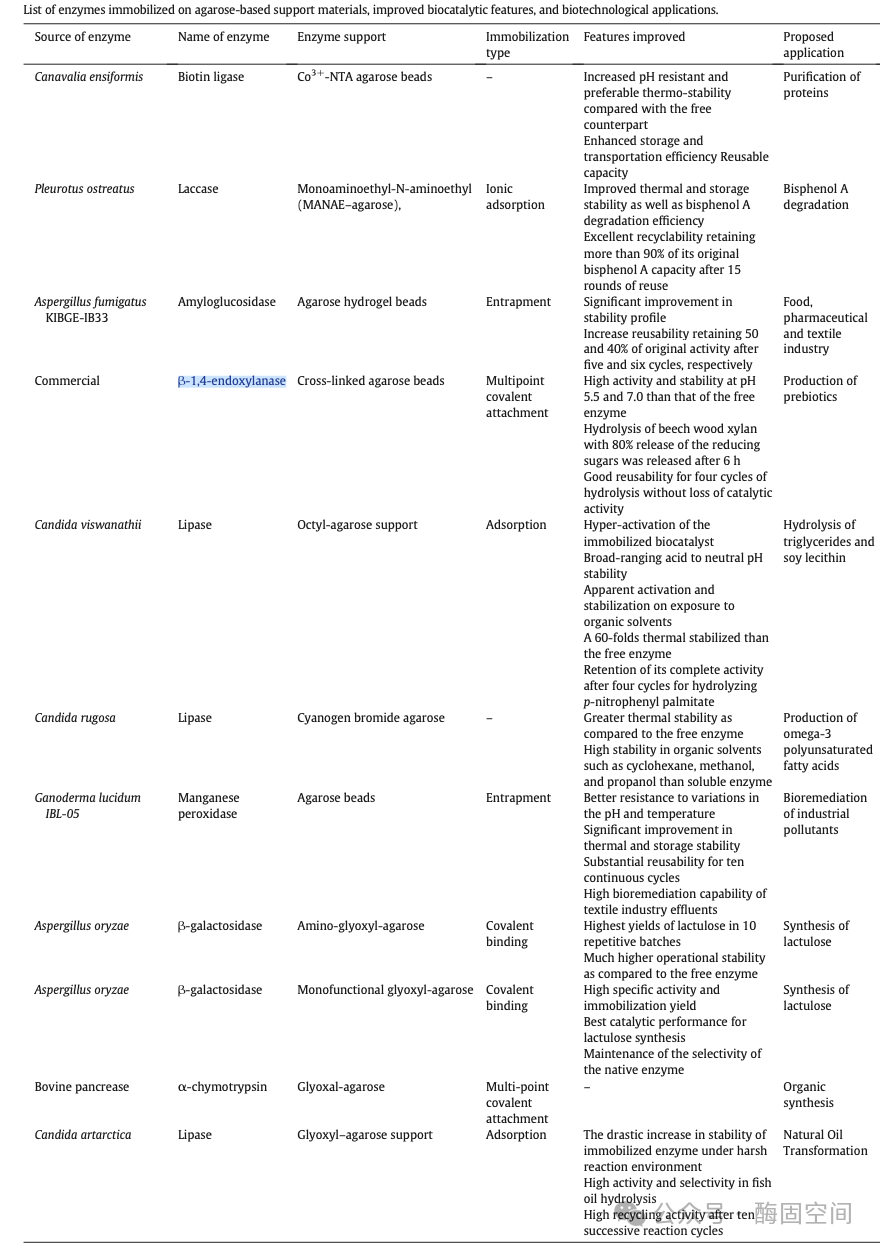
琼脂糖固定化酶载体可应用于食品、医药、环境等各个领域,选择合适的琼脂糖固定化酶载体是其成功应用于各行业的基础之一,表1为综述[8]中整理的琼脂糖在各领域的应用,可见此类载体在实际应用中的通用性和可靠性。
表1 琼脂糖固定化酶载体的应用示例[8]
琼脂糖科技:提供值得信赖的琼脂糖固定化酶载体解决方案。
基于对琼脂糖固定化酶载体特性与构效关系的理解,琼脂糖科技可提供高品质的琼脂糖基质产品,为您构建高效、稳定的固定化酶体系提供可靠的基础材料支持。
专注基础:提供粒径分布在100-200微米、符合琼脂糖经典优良特性的载体。
规格明确:提供标准化的粒径选项,清晰的孔径、耐压信息,以及多样化的活化基团(氨基、金属螯合、NHS、重氮基团)以满足不同的固定化策略。
质量可靠:严格执行生产工艺与质量控制流程,致力于保障批次间一致性,为您的实验或工艺提供稳定的起点。
专业支持:我们的团队可提供基于文献和我们产品特性的初步选型建议,助您匹配需求。
如需了解特定应用场景的选型建议或对我们的产品感兴趣,请联系我们。
[1] 曹林秋.载体固定化酶——原理,应用和设计.北京:化学工业出版社, 2008.
[2] Paolo Zucca, Roberto Fernandez-Lafuente and Enrico Sanjust. Agarose and Its Derivatives as Supports for Enzyme Immobilization. Molecules. 2016(21): 1577.
[3] Jose C.S dos Santos, et al. Characterization of supports activated with divinyl sulfone as a tool to immobilize and stabilize enzymes via multipoint covalent attachment. Application to chymotrypsin. RSC Advances. 2015.
[4] Nicole A. Montoya, et al. Review on porous materials for the thermal stabilization of proteins. Microporous and Mesoporous Materials. 2022(333): 111750.
[5] Marina Simona Robescu and Teodora Bavaro. A Comprehensive Guide to Enzyme Immobilization: All You Need to Know. Molecules. 2025(30): 939.
[6] Pawan Gupta, Tariq Maqbool , M. Saleemuddin. Oriented immobilization of stem bromelain via the lone histidine on a metal affinity support. Journal of Molecular Catalysis B: Enzymatic. 2007(45): 78.
[7] Cesar Mateo, et al.Some special features of glyoxyl supports to immobilize proteins. Enzyme and Microbial Technology 2005(37): 456–462.
[8] Muhammad Bilal, Hafiz M.N. Iqbal. Naturally-derived biopolymers: Potential platforms for enzyme immobilization. International Journal of Biological Macromolecules. 2019(130): 462-482.
- 上一篇:蛋白纯化中的内毒素去除方法介绍 2025/12/30
- 下一篇:琼脂糖在美容填充领域应用的行业研究|行业研究 2025/12/27
