生物分离纯化工艺基础:从原理到精准分离
第一章:层析技术的原理与分类
所有纯化工艺的底层逻辑,都建立在利用目标分子与杂质之间固有的物理化学性质差异之上。层析技术,作为主流的分离手段,正是通过设计与这些差异相匹配的相互作用,实现精准分离。
五大核心技术:
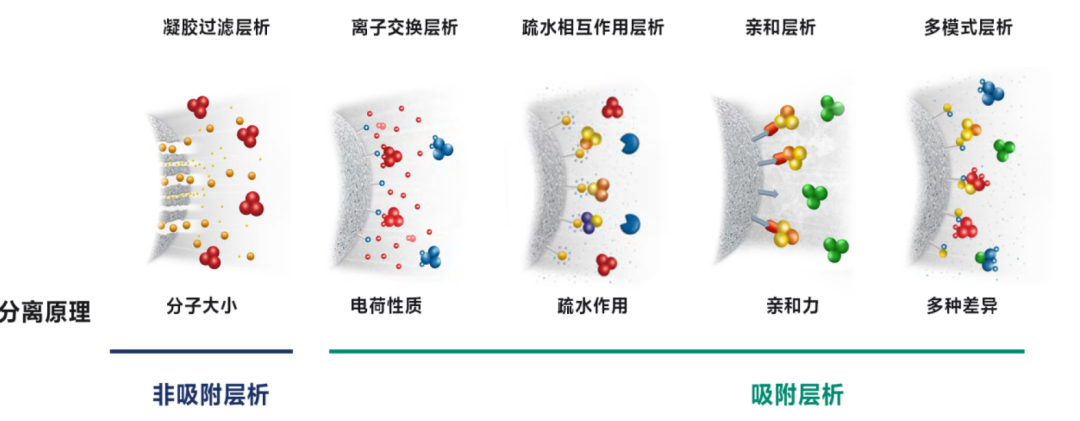
针对不同维度的差异生物分子间的主要差异可归纳为分子大小、电荷、疏水性、生物特异性,据此衍生出五大类层析技术:
1. 凝胶过滤层析:依据分子大小与形状差异。大分子无法进入填料孔内,先流出;小分子进入孔内,流经路径长,后流出。
核心应用: 脱盐、缓冲液置换、去除聚集体、分子量测定。
2. 离子交换层析:依据分子表面净电荷差异。通过改变缓冲液pH(决定分子带电状态)和盐浓度(竞争性洗脱),实现分离。
核心应用: 应用最广的捕获与中度纯化技术,适用于绝大多数带电分子。
3. 疏水相互作用层析:依据分子表面疏水区差异。在高盐环境下增强疏水相互作用实现结合,降低盐浓度进行洗脱。
核心应用: 分离疏水性强的分子,常与离子交换技术互补使用。
4. 亲和层析:依据生物特异性相互作用(如抗原-抗体、酶-底物、配体-受体)。利用高特异性、高亲和力的配基进行“一对一”捕获。
核心应用: 高选择性捕获步骤的黄金标准,如抗体Protein A纯化、His标签蛋白纯化。
5. 复合模式层析:整合两种及以上相互作用力于单一填料(如离子交换+疏水作用)。提供独特的选择性,可一步去除多种杂质,或在高盐条件下直接上样。
核心应用: 工艺强化和简化,如抗体精纯、复杂样品的直接捕获。
分离效能的核心载体:
层析填料所有层析技术的效能最终落脚于层析填料这一精密工具。其结构设计直接决定了分离的选择性、载量和分辨率。
基架:多孔微球的“骨架”。材质(如琼脂糖的生物相容性、聚合物的高刚性)决定了填料的化学物理稳定性及耐受能力;粒径(如34μm、90μm)直接影响分辨率与系统反压。
连接臂:连接基架与配基的化学“手臂”。其长度与化学性质至关重要,能有效减少空间位阻,尤其当配基或目标分子较大时,能显著提高结合效率与有效载量。
配基:负责与目标分子特异性结合的“触手”。其类型(如阴离子交换配基Q、疏水配基Phenyl、亲和配基Protein A)直接定义层析的类型和选择性。

第二章:离子交换层析详解——电荷差异的精细操控
离子交换层析(IEX)是纯化流程中最通用、最核心的技术之一。其本质是一个动态的静电吸附与竞争性洗脱过程,基本步骤与动态过程。
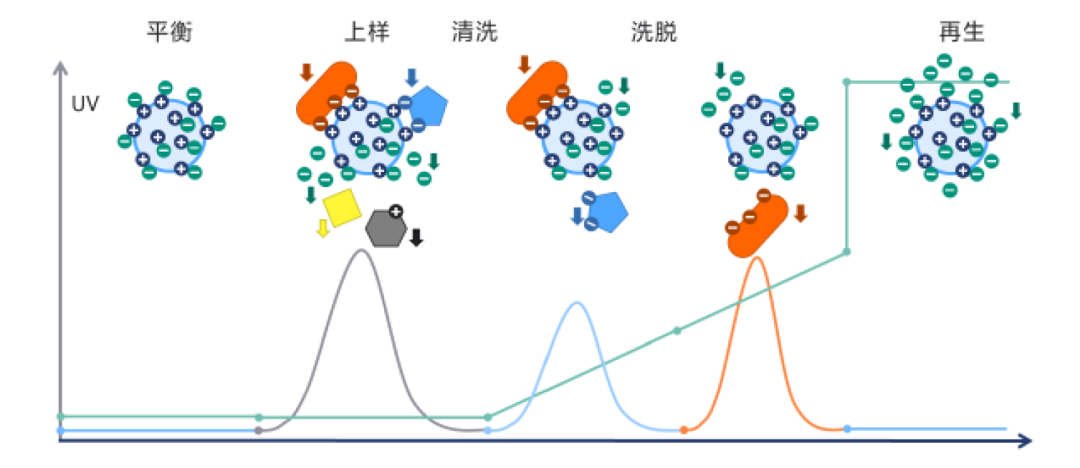
平衡:用低离子强度缓冲液平衡柱子,确保填料配基完全带电并准备好结合。
上样:在低盐条件下,带相反电荷的目标分子与杂质被吸附到填料上。
清洗:用平衡缓冲液或略高盐缓冲液洗去未结合或弱结合的杂质。
洗脱:通过线性或阶梯式增加盐浓度(如NaCl梯度),带电量不同的分子按结合力强弱依次被竞争下来,实现分离。pH梯度洗脱是另一种选择,通过改变分子自身电荷实现洗脱。
再生与保存:用高盐或极端pH溶液彻底清洗填料,恢复其结合能力,并置于保存液中。
离子交换核心载体:阴离子交换柱
固定相通常由带正电荷的基团(如季铵盐)键合到硅胶或聚合物基质上构成。寡核苷酸的磷酸骨架在常规纯化pH(6-9)下完全带负电荷,因此会与固定相上的正电荷发生强烈的静电吸附。
差异吸附与洗脱
结合强度:在相同条件下,长链寡核苷酸比短链带有更多的负电荷。因此,全长产物(n-mer)与固定相结合得比短链失败序列(n-1, n-2...)更牢固。
洗脱顺序:当增加流动相中的竞争性阴离子浓度(通常是盐,如NaClO₄或NaCl)时,结合较弱的短片段会先被置换下来,随后才是结合更强的长片段。
分离结果:最终实现按链长(即电荷数)从短到长的顺序洗脱,这是分离全长产物与“n-1”等缺失片段最理想的机制。
直接针对主要杂质:化学合成的主要失败产物就是因偶联效率不足而产生的“n-1”片段。IEX基于链长/电荷数的分离模式,能最直接、最有效地将全长产物与这些短一个或多个核苷酸的杂质分离开。 适用于未修饰及普通修饰产物:对于不带强疏水修饰的DNA或RNA,尤其是长度超过30个碱基的寡核苷酸,IEX的分辨率通常高于反相HPLC。反相HPLC主要基于碱基的疏水性,对长链寡核苷酸链长差异的区分能力有限。 高载量:相比反相柱,离子交换柱通常具有更高的样品载量,适合制备级纯化。
缓冲液、pH与盐梯度的选择策略,缓冲液与pH的选择:控制电荷状态与分辨率,目标pH范围:7.0 - 8.5。在此范围内,寡核苷酸的磷酸基团完全解离(带负电),确保其与固定相稳定结合。同时,此pH范围也能防止碱基发生脱嘌呤等副反应。
常用缓冲体系
磷酸盐缓冲液(如NaH₂PO₄/Na₂HPO₄):兼容性好,是经典选择。
盐(洗脱剂)的选择:实现梯度洗脱,作用:盐中的阴离子(如ClO₄⁻, Cl⁻)作为竞争剂,与寡核苷酸竞争结合固定相上的正电荷位点,从而实现洗脱。
高氯酸钠:洗脱能力强,分辨率高,是实验室常用选择。
氯化钠:洗脱能力较弱,但更温和、更安全,尤其适合后续需进行质谱分析或大规模制备。
浓度:通常以 1.0 - 2.0 M 的高浓度储备液形式加入流动相B中。
梯度设计:平衡分辨率与时间起始浓度:流动相A(低盐缓冲液)中的盐浓度通常很低(如20-50 mM),以确保样品能牢固吸附在柱头。
梯度斜率
分析/小规模制备:采用较缓的线性梯度(例如,30分钟内盐浓度从0% B升至50% B)。梯度越缓,分辨率越高,分离效果越好,但耗时更长。
大规模制备:可能采用阶梯式或较陡的梯度以提高效率,但会牺牲部分分辨率。
通用起始条件
示例:柱温:50-60°C(可减少二级结构,使分离完全基于链长)。
流动相A:20 mM 磷酸钠缓冲液 (pH 7.0)。
流动相B:20 mM 磷酸钠缓冲液 (pH 7.0) + 1.0 M NaCl。
梯度:0-30分钟,0% → 50% B。
流速:根据柱规格设定(如1.0 mL/min for 4.6 mm ID柱)
第三章:纯化策略的构建——从目标到路线图
纯化实验前准备:
明确纯化目标:终产物的用途决定质量要求。用于质谱鉴定,微克级、>80%纯度即可;用于治疗,则需克级规模、>90%纯度、高活性与均一性。
了解目标分子性质:详细表征分子量、pI、稳定性(pH、温度、氧化、还原)等。例如,pI指导离子交换填料类型和pH条件;稳定性范围限定所有操作条件。
分析起始物料:明确样品来源(如大肠杆菌、CHO细胞)、体积、浓度、关键杂质(宿主蛋白、DNA、内毒素)等,以设计必要的前处理步骤(离心、过滤、稀释)。

CIPP纯化策略:三步走的艺术
一个稳健的纯化流程通常分三步走,旨在平衡效率、纯度与回收率:
捕获:目标是从大体积、成分复杂的料液中快速浓缩、富集目标物,去除大部分杂质。高载量、高流速的技术是首选,如亲和层析或离子交换层析。
中度纯化:任务是去除与目标物性质相近的关键杂质(如宿主细胞蛋白、核酸、病毒)。高分辨率的技术在此阶段发挥核心作用,如离子交换、疏水层析或复合模式层析。
精细纯化:最后一步是“抛光”,去除痕量杂质(如聚集体、内毒素)并将样品置换到最终制剂缓冲液中。凝胶过滤层析是此阶段的金标准,因其条件温和且能有效去除聚集体。
结语
纯化工艺的核心,在于深刻理解并精巧利用目标分子与杂质之间多维度的性质差异,通过选择与组合具有互补选择性的层析技术,构建一道从捕获、中度纯化到精细纯化的精密质量闸门。从通用的蛋白质纯化,到极限挑战的核酸药物分离,这一核心逻辑一脉相承。掌握从分子性质分析、技术原理理解到填料科学选择和工艺策略构建的完整知识链,是开发生物药高效、稳健、可放大纯化工艺的根本。
参考文献:
G. R. Gough, M. J. Gait Current Protocols in Nucleic Acid Chemistry (2002) 《Oligonucleotide synthesis and purification》
- 上一篇:蛋白纯化过程中常用的蛋白酶抑制剂及其使用 2025/12/13
- 下一篇:用琼脂创作细菌画是一门优雅但危险的艺术 2025/12/12
